24小时服务热线
13007546599
服务热线:13007546599
服务项目
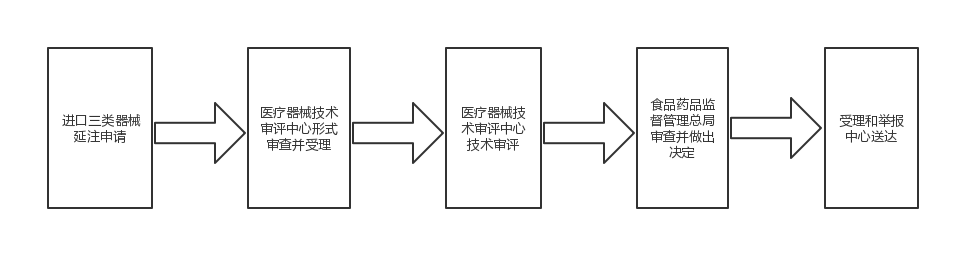
Products Classification申请人应为境外依法进行登记的生产企业,且该医疗器械已在注册申请人注册地或者生产地址所在国家(地区)已获准上市销售。
1、注册人未在规定时限内提出延续注册申请的;
2、医疗器械强制性标准已经修改,该医疗器械不能达到新要求的;
3、对用于治疗罕见疾病以及应对突发公共卫生事件急需的医疗器械,批准注册部门在批准上市时提出要求,注册人未在规定期限内完成医疗器械注册证载明事项的。
1、申请表;
2、证明性文件;
境外注册人应当提交其在中国指定代理人的委托书、代理人承诺书及营业执照副本复印件或者机构登记证明复印件。
注:进口医疗器械延续注册时,不需要提供注册人注册地或者生产地址所在国家(地区)批准产品上市销售的证明文件。
3、关于产品没有变化的声明:注册人提供产品没有变化的声明。
4、原医疗器械注册证及其附件的复印件、历次医疗器械注册变更文件复印件。
5、注册证有效期内产品分析报告
(1)产品临床应用情况,用户投诉情况及采取的措施。
(2)医疗器械不良事件汇总分析评价报告,报告应对本产品上市后发生的可疑不良事件列表、说明在每一种情况下生产企业采取的处理和解决方案。对上述不良事件进行分析评价,阐明不良事件发生的原因并对其安全性、有效性的影响予以说明。
(3)产品市场情况说明。
(4)产品监督抽验情况(如有)。
(5)如上市后发生了召回,应当说明召回原因、过程和处理结果。
(6)原医疗器械注册证中载明要求继续完成工作的,应当提供相关总结报告,并附相应资料。
6、产品检验报告
如医疗器械强制性标准已经修订,应提供产品能够达到新要求的产品检验报告。产品检验报告可以是自检报告、委托检验报告或符合强制性标准实施通知规定的检验报告。其中,委托检验报告应由具有医疗器械检验资质的医疗器械检验机构出具。
7、符合性声明
(1)注册人声明本产品符合《医疗器械注册管理办法》和相关法规的要求;声明本产品符合现行国家标准、行业标准,并提供符合标准的清单。
(2)所提交资料真实性的自我保证声明(进口产品由注册人和代理人分别出具)。
8、其他
如在原医疗器械注册证有效期内发生了涉及产品技术要求变更的,应当提交依据注册变更文件修改的产品技术要求一式两份。
1、注册人关于产品没有变化的声明;
2、原医疗器械注册证机器附件复印件;
3、历次医疗器械注册变更文件复印件;
4、注册证有效期内产品分析报告;
(1)产品临床应用情况,用户投诉情况及采取的措施。
(2)医疗器械不良事件汇总分析评价报告,报告应对本产品上市后发生的可疑不良事件列表、说明在每一种情况下生产企业采取的处理和解决方案。对上述不良事件进行分析评价,阐明不良事件发生的原因并对其安全性、有效性的影响予以说明。
(3)产品市场情况说明。
(4)产品监督抽验情况(如有)。
(5)如上市后发生了召回,应当说明召回原因、过程和处理结果。
(6)原医疗器械注册证中载明要求继续完成工作的,应当提供相关总结报告,并附相应资料。
5、注册证有效期内发生涉及产品技术要求变更的,提交根据变更文件修改的产品说明书和/或产品技术要求各一式两份;
(1)产品型号/规格及其划分说明。
(2)性能指标。
(3)检验方法。
(4)附录。
6、产品检验报告;
如医疗器械强制性标准已经修订,应提供产品能够达到新要求的产品检验报告。产品检验报告可以是自检报告、委托检验报告或符合强制性标准实施通知规定的检验报告。其中,委托检验报告应由具有医疗器械检验资质的医疗器械检验机构出具。
7、境外注册人在中国境内指定代理人的委托书;
8、代理人承诺书;
9、代理人营业执照副本或者机构登记证明复印件;
10、符合性声明和符合标准的清单;
11、申请人所在地公证机构出具的公证件。
| 主管部门 | 管理类别 | 首次注册 |
注册变更 (许可事项变更) |
延续注册 (五年一次) |
临床试验申请费 (高风险医疗器械) |
相关文件 | 实施日期 | ||
|---|---|---|---|---|---|---|---|---|---|
| 国家局 | 境外 | Ⅲ | 30.88 | 5.04 | 4.08 | 4.32 | 国家局2015年53号 | 2015/5/27 | |
| 文件名称 | 文号 |
|---|---|
| 《医疗器械监督管理条例》 | 650号文件 |
| 《医疗器械注册管理办法》 | 局令4号 |
| 《中华人民共和国行政许可法》 | 局令6号 |
| 进口医疗器械注册审批—进口医疗器械延续注册审批服务指南 | 30017 |
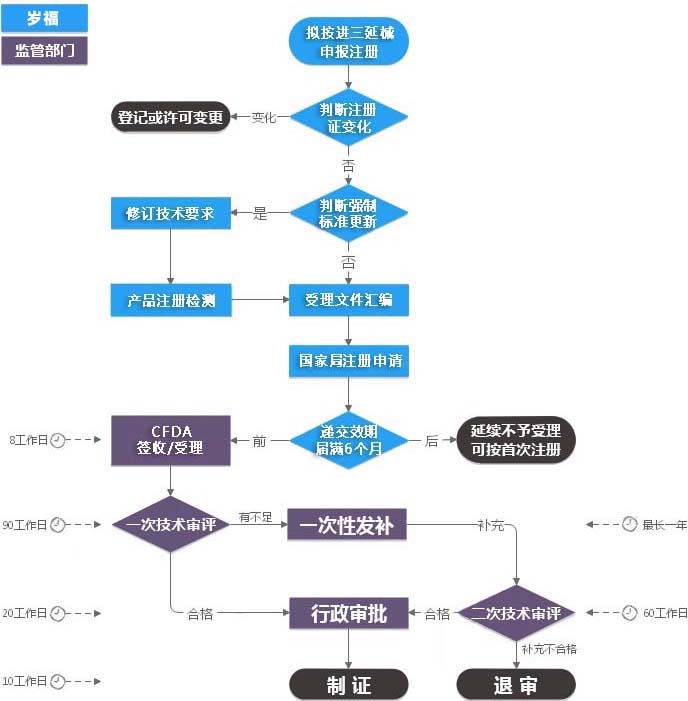
立项阶段
预算、合同、考虑期,7个工作日。
受理前资料准备
视产品情况有所变化,如无强标更新,则可免除检测。考虑检测平均消耗6个月。
如需精算请联络思途。(免临床目录产品除外。)
注册资料编制可与检测并行,递交后5个工作日内受理。
受理后
CFDA法定消耗预算20-30个工作日。(不计节假,不含技术审评和申请人补充资料及补充资料审评所需的时间)
发补时限0~6个月,考虑平均时间3个月。视产品首次申报资料情况而定。
审批行政结果送达申请人10个工作日。
预算合计
进口三类医疗器械证延续注册,预算应至少3.5~10个月以上。
| 进口三类医疗器械注册服务 | 医疗器械临床试验服务 |
| 注册英文文件翻译 | 创新医疗器械审批申请服务 |
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
河南岁福医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、GMP质量辅导等方面的技术外包和生产许可证、经营许可证及临床机构备案办理服务。

下一篇:没有了