24小时服务热线
13007546599
服务热线:13007546599
服务项目
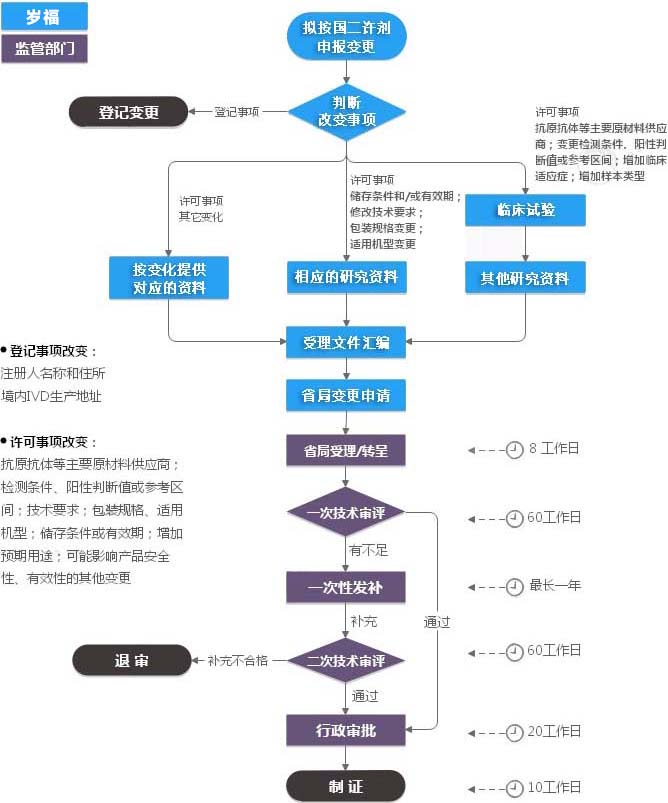
Products Classification已注册的第二类体外诊断试剂,医疗器械注册证及其附件载明的内容发生变化,注册人应当向原注册部门申请注册变更,并按照相关要求提交申报资料。 注册证及附件载明内容发生以下变化的,申请人应当向原注册部门申请许可事项变更。境内第二类体外诊断试剂注册变更由省、自治区、直辖市食品药品监督管理部门审查。
1、抗原、抗体等主要材料供应商变更的;
2、检测条件、阳性判断值或者参考区间变更的;
3、注册产品技术要求内容变更;
4、包装规格变更;
5、适用机型变更;
6、产品储存条件或者产品有效期变更的;
7、预期用途表更;
8、产品名称变更;
9、产品说明书变更;
10、可能影响产品安全性、有效性的其他变更。
1、《体外诊断试剂注册变更申请表》(许可事项);
2、证明性文件;
3、注册人关于变更情况的声明;
4、原医疗器械注册证及其附件复印件、历次医疗器械注册变更文件复印件;
5、变更申请项目申报技术资料的要求(资料中涉及需要提交产品技术要求、说明书的,另需提交Word文档形式的电子文本);
6、符合性声明;
7、申办人身份证复印件。申办人不是营业执照载明的法定代表人或负责人的,应提交法定代表人或负责人的授权委托书。
| 主管部门 | 管理类别 | 首次注册 |
注册变更 (许可事项变更) |
延续注册 (五年一次) |
实施日期 | ||
|---|---|---|---|---|---|---|---|
|
省 局 |
1 | 福建省 | Ⅱ | 5.77 | 2.42 | 2.39 | 2018/9/11 |
| 2 | 江西省 | Ⅱ | 5.467 | 2.289 | 2.268 | 2020/2/6 | |
| 3 | 上海市 | Ⅱ | 6.573 | 2.751 | 2.73 | 2018/5/9 | |
| 4 | 海南省 | Ⅱ | 5.81 | 2.408 | 2.387 | 2020/5/27 | |
| 5 | 山东省 | Ⅱ | 5.754 | 2.408 | 2.387 | 2020/08/21 | |
| 6 | 安徽省 | Ⅱ | 5.005 | 2.093 | 2.079 | 2019/10/22 | |
| 7 | 浙江省 | Ⅱ | 6.573 | 2.2008 | 2.184 | 2020/7/1至2020/12/31 | |
| 8 | 山西省 | Ⅱ | 4.2315 | 1.6275 | 1.6275 | 2020/4/16 | |
| 9 | 云南省 | Ⅱ | 4.28 | 1.75 | 1.75 | 2018/3/16 | |
| 10 | 河北省 | Ⅱ | 7.23 | 3.03 | 3 | 2016/10/1 | |
| 11 | 江苏省 | Ⅱ | 5.915 | 2.471 | 2.457 | 2019/2/13 | |
| 12 | 宁夏 | Ⅱ | 1.5 | 0.65 | 0.65 | 2019/12/18 | |
| 13 | 黑龙江 | Ⅱ | 5.76 | 2.416 | 2.4 | 2017/8/1 | |
| 14 | 广东省 | Ⅱ | 5.726 | 2.394 | 2.38 | 2019/2/25 | |
| 15 | 湖南省 | Ⅱ | 5.04 | 2.114 | 2.1 | 2019/4/11 | |
| 16 | 四川省 | Ⅱ | 3.95 | 1.65 | 1.65 | 2019/11/27 | |
| 17 | 贵州省 | Ⅱ | 4.29 | 1.76 | 1.76 | 2017/10/17 | |
| 18 | 广西 | Ⅱ | 7.57 | 3.16 | 3.14 | 2017/12/29 | |
| 19 | 辽宁省 | Ⅱ | 5 | 2.1 | 2.1 | 2020/6/12 | |
| 20 | 吉林省 | Ⅱ | 0 | 0 | 0 | 2020/2/8 | |
| 21 | 湖北省 | Ⅱ | 0 | 0 | 0 | ||
| 22 | 河南省 | Ⅱ | 0 | 0 | 0 | ||
| 23 | 重庆市 | Ⅱ | 0 | 0 | 0 | 2019/5/15 | |
| 24 | 甘肃省 | Ⅱ | 0 | 0 | 0 | ||
| 25 | 新疆 | Ⅱ | 0 | 0 | 0 | ||
| 26 | 内蒙古 | Ⅱ | 0 | 0 | 0 | 2019/9/17 | |
| 27 | 北京市 | Ⅱ | 0 | 0 | 0 | 2019/4/25 | |
| 28 | 天津市 | Ⅱ | 0 | 0 | 0 | 2019/1/4 | |
| 29 | 陕西省 | Ⅱ | 0 | 0 | 0 | 2020/1/10 | |
| 文件名称 | 文号 |
|---|---|
| 《医疗器械监督管理条例》 | 650号文件 |
| 《体外诊断试剂注册管理办法》 | 局令5号 |
| 《关于公布体外诊断试剂注册申报资料要求和批准证明文件格式的公告》 | 总局公告2014年44号 |
| 食品药品监管总局关于印发境内第二类医疗器械注册审批操作规范的通知 | 食药监械管〔2014〕209号 |
立项阶段
预算、合同、考虑期,1个月。
受理前资料准备
资料提供,视客户情况而定 1个月
*如需:产品检测,视产品情况有所变化。 *平均3个月
*如需:临床实验不可与检测并行,临床应单独核算时间。 *至少6个月
变更资料编制(可与检测或临床并行。) 1个月
受理后
CFDA法定消耗预算5个月。(98工日,20工日/月,不计节假) 至少5个月
*发补(如适用):1、发补资料准备时限0~12个月视产品递交的申报资料情况而定。 *平均6个月
*发补(如适用):2、发补技术评审时间预计消耗3个月(60工作日) *3个月
*如需:体系考核,注册受理后,额外30工作日 *1.5个月
预算合计
无需重新检测、临床、体考、发补 预算平均8个月
| 许可事项变更资料汇编服务 | 汇编资料申报服务 |
| 省药监局跑腿代办服务 | 延伸:ivd临床试验服务 |
| 延伸:GMP年度辅导服务 | 延伸:二类ivd产品注册服务 |
站点声明:
本网站所提供的信息仅供参考之用,并不代表本网赞同其观点,也不代表本网对其真实性负责。图片版权归原作者所有,如有侵权请联系我们,我们立刻删除。如有关于作品内容、版权或其它问题请于作品发表后的30日内与本站联系,本网将迅速给您回应并做相关处理。
河南岁福医疗科技有限公司专注于医疗器械、诊断试剂产品政策与法规规事务服务,提供产品注册申报代理、临床合同(CRO)研究、GMP质量辅导等方面的技术外包和生产许可证、经营许可证及临床机构备案办理服务。